Le côlon humain héberge des centaines de milliards de micro-organismes, formant un écosystème d’une complexité remarquable, caractérisé par une très forte variabilité individuelle. Notre microbiote est aujourd’hui considéré comme un organe à part entière, impliqué dans des processus allant bien au-delà de la digestion.
|
100 000
milliardsde bactéries hébergées |
800–1000espèces différentes
|
~1 kgde la masse corporelle
|
70%du système immunitaire est intestinal
|
Que sont les probiotiques, prébiotiques et symbiotiques ?
Selon la définition de l’OMS (2001), les probiotiques sont des micro-organismes vivants qui, lorsqu’ils sont ingérés en quantité suffisante, exercent des effets bénéfiques sur la santé de l’hôte, au-delà des effets nutritionnels traditionnels. Les plus connus sont les Lactobacillus, les Bifidobacterium et la levure Saccharomyces boulardii.
Les prébiotiques sont des fibres alimentaires non digestibles (inuline, FOS, GOS…) qui servent de substrat sélectif aux bactéries bénéfiques du microbiote. Les aliments naturellement riches en prébiotiques : artichaut, ail, oignon, asperges, bananes, avoine, légumineuses.
Les symbiotiques associent probiotiques et prébiotiques dans un même produit, renforçant leur efficacité combinée.
Conditions requises pour qu’un probiotique soit efficace
|
✔ Qualités indispensables
• Non pathogène et non toxique |
⚠ Points de vigilance
• Tous les probiotiques ne sont pas équivalents : l’efficacité dépend de la souche précise, de la dose et de la durée |
L’axe intestin-cerveau Nouveauté
L’intestin : notre « deuxième cerveau »
L’axe intestin-cerveau désigne un réseau de communication bidirectionnel entre le système digestif et le système nerveux central. Cette communication s’effectue via quatre grandes voies :
| 🔌 Voie nerveuse Le nerf vague constitue l’autoroute principale entre intestin et cerveau. Le système nerveux entérique (SNE) contient plus de 100 millions de neurones — autant que la moelle épinière. |
🧪 Voie hormonale Les cellules entérochromaffines de la muqueuse intestinale produisent 90% de la sérotonine de l’organisme sous l’influence des métabolites bactériens. |
| 🛡️ Voie immunitaire Le microbiote interagit en permanence avec les cellules immunitaires intestinales, qui transmettent des signaux au cerveau via les cytokines. |
🩸 Voie métabolique Les métabolites bactériens (AGCC, neuropeptides) passent dans la circulation sanguine et peuvent agir directement sur le cerveau. |
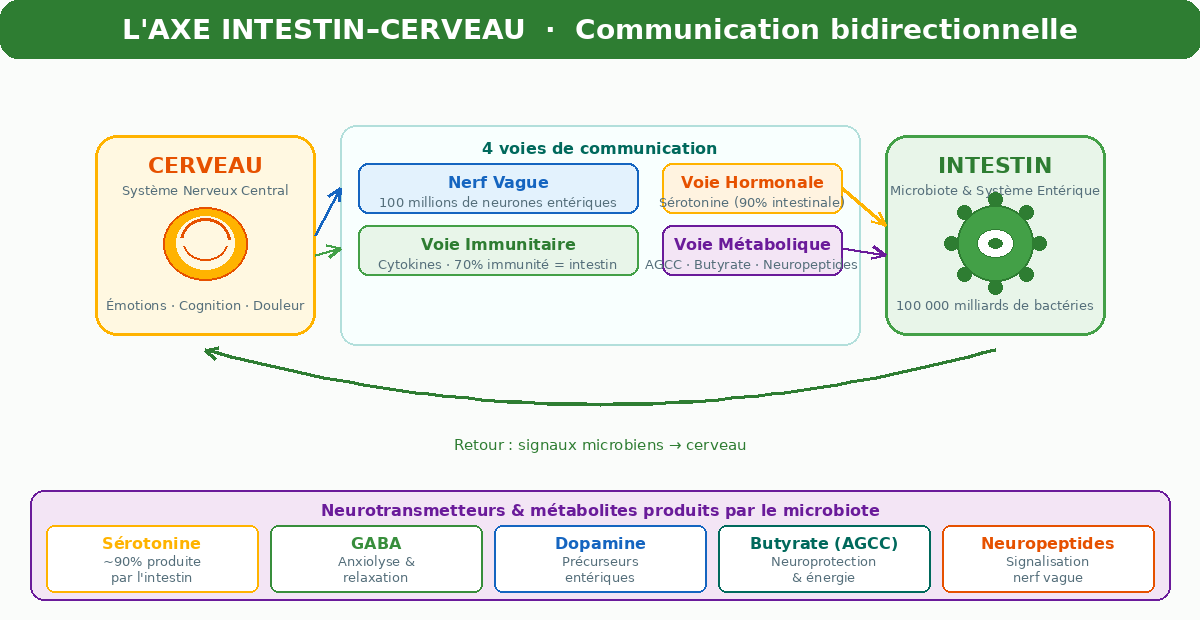
Schéma de l’axe intestin-cerveau — communication bidirectionnelle (© pharmaciedelepoulle.com)
Neurotransmetteurs synthétisés par le microbiote intestinal
| Neurotransmetteur | Part produite par l’intestin | Rôle principal | Souches impliquées |
|---|---|---|---|
| Sérotonine | ~90% de la sérotonine totale | Humeur, sommeil, transit intestinal | L. helveticus, B. longum |
| GABA | Production intestinale significative | Anxiolyse, relaxation | L. rhamnosus, L. brevis |
| Dopamine (précurseur) | Précurseurs intestinaux | Motivation, plaisir, mouvement | L. plantarum PS128 |
| Butyrate (AGCC) | 100% production microbienne | Neuroprotection, énergie des colonocytes, barrière intestinale | Faecalibacterium prausnitzii, Roseburia |
Les psychobiotiques 2024–2025
Une nouvelle classe thérapeutique prometteuse
Le terme psychobiotique a été défini pour la première fois en 2013 par les psychiatres Dinan et Cryan. Il désigne des micro-organismes vivants ayant un impact bénéfique démontré sur la santé mentale via l’axe intestin-cerveau. Tous les probiotiques ne sont pas psychobiotiques, et tous les psychobiotiques ne sont pas des probiotiques classiques.
Ils agissent sur le SNC par des voies immunitaires, hormonales, neuronales et métaboliques. Les données récentes publiées dans Actualités Pharmaceutiques (2025) confirment leur potentiel dans plusieurs pathologies psychiatriques et neurodégénératives.
| Souche psychobiotique | Indication principale | Données cliniques |
|---|---|---|
| L. helveticus R0052 + B. longum R0175 | Anxiété, stress, qualité du sommeil | Méta-analyse 2024 (n>3000) : réduction significative de l’anxiété en 4 semaines |
| Bifidobacterium longum 1714 | Stress, mémoire | Diminue le stress perçu, améliore la mémoire visuospatiale chez des adultes sains |
| L. plantarum PS128 | Stress, anxiété, dépression légère | Réduit le stress et l’anxiété chez les sujets très stressés ; piste dans la maladie de Parkinson |
| L. helveticus R0052 + B. longum | Dépression majeure | Réduction des scores de dépression en association avec traitement classique |
| L. casei Shirota | Stress académique | Prévention des symptômes physiques lors de stress intense (étude sur étudiants) |
📰 Étude marquante 2024 (Institut du Cerveau / PNAS Nexus)
Une étude publiée en mai 2024 dans PNAS Nexus par des chercheurs de l’Institut du Cerveau (Paris) et l’Université de Bonn a montré que des modifications du microbiote intestinal pouvaient influencer la prise de décision sociale. Après 7 semaines de supplémentation en probiotiques et prébiotiques, les participants montraient une sensibilité significativement accrue à l’injustice par rapport au groupe placebo — témoignant d’un impact sur les processus cognitifs et émotionnels complexes.
Falkenstein M. et al. Impact of the Gut Microbiome Composition on Social Decision-Making. PNAS Nexus, Mai 2024. DOI: 10.1093/pnasnexus/pgae166
Microbiote et maladies neurodégénératives Nouveauté
Maladie de Parkinson
Des travaux récents confirment que la dysbiose joue un rôle central dans la maladie de Parkinson. On observe chez les patients parkinsoniens une augmentation des bactéries pro-inflammatoires et une diminution des bactéries anti-inflammatoires. Cette dysbiose favorise l’inflammation intestinale et, selon l’hypothèse de Braak, pourrait faciliter l’accumulation d’agrégats d’alpha-synucléine dans les neurones entériques qui migreraient ensuite vers le cerveau via le nerf vague. Des études précliniques (2025) sur Lactiplantibacillus plantarum montrent des effets protecteurs sur la barrière intestinale et la neuroinflammation dans des modèles murins.
Maladie d’Alzheimer
Les patients Alzheimer présentent un microbiote appauvri en bactéries productrices de butyrate et enrichi en bactéries pro-inflammatoires. Une méta-analyse portant sur 4 275 personnes de plus de 45 ans (compilation de 15 études, 2012-2025) montre qu’une supplémentation en probiotiques et symbiotiques est associée à une amélioration modérée des fonctions exécutives et du langage. Des essais contrôlés randomisés de grande envergure sont encore nécessaires.
Syndrome de l’intestin irritable (SII) et axe cerveau-intestin
Le SII est désormais classé par Rome IV comme un « désordre des interactions de l’axe cerveau-intestin ». Des données récentes (FMC-HGE, 2024) ont mis en évidence une signature multi-omique du microbiome propre aux différents sous-types de SII, et une altération de la connectivité cérébrale liée à la composition du microbiote. Les probiotiques constituent aujourd’hui une stratégie thérapeutique validée dans cette indication, même si l’efficacité reste souche-dépendante.
Comment agissent les probiotiques ?
Effet barrière contre les pathogènes
Les probiotiques produisent des acides organiques (lactique, acétique) qui abaissent le pH intestinal, inhibant E. coli et les Salmonelles. Ils sécrètent des bactériocines antimicrobiennes, déconjuguent les sels biliaires et exercent une inhibition compétitive vis-à-vis des germes pathogènes sur les sites d’adhésion muqueux.
Amélioration de la digestibilité
Les Lactobacillus excrètent la β-galactosidase, facilitant la digestion du lactose. Ils stimulent les activités lactase, invertase et maltase des cellules épithéliales et améliorent l’assimilation des acides aminés essentiels.
Rôle nutritionnel
Les bifidobactéries synthétisent vitamines (B1, B2, B9) et acides aminés (alanine, thréonine, valine). Les acides gras volatils produits par fermentation (acétate, propionate, butyrate) constituent une source d’énergie pouvant représenter jusqu’à 10% des apports énergétiques en période de restriction calorique. Le butyrate joue de surcroît un rôle neuroprotecteur et renforce la barrière intestinale.
Stimulation de l’immunité
70% du système immunitaire est d’origine intestinale. Les probiotiques activent les macrophages, augmentent la production d’IgA sécrétoires (première ligne de défense muqueuse) et modulent la balance Th1/Th2, réduisant ainsi les phénomènes inflammatoires chroniques et allergiques.
Équilibre nerveux et axe intestin-cerveau
Le cerveau peut moduler la composition du microbiote via le transit et les influx nerveux entériques. En retour, le microbiote fabrique des neuropeptides et stimule la production de neurotransmetteurs (sérotonine, GABA) qui remontent vers le cerveau par le nerf vague. Cette communication joue un rôle fondamental dans la perception de la douleur, la gestion des émotions et la régulation immunitaire.
Indications thérapeutiques
Immunité
Les souches à privilégier pour stimuler le système immunitaire sont Lactobacillus casei, L. acidophilus, L. rhamnosus et Bifidus. Elles améliorent la détection macrophagique, stimulent la production d’immunoglobulines et renforcent la réactivité lymphocytaire.
Troubles digestifs
Diarrhées infectieuses : L. casei, L. GG, Bifidobacterium breve et B. longum réduisent la durée et l’intensité, notamment chez l’enfant. L. GG réduit l’incidence de la diarrhée du voyageur de près de 40%. En cas de diarrhée à Clostridium difficile post-antibiotique, L. GG est particulièrement indiqué.
Constipation : L. acidophilus et Bifidobacterium réduisent le recours aux laxatifs en rééduquant le transit.
Intolérance au lactose : L. bulgaricus, L. acidophilus et S. thermophilus produisent la β-galactosidase, facilitant la digestion du lactose.
Ballonnements : cure de 2 mois recommandée. H. pylori : l’association de probiotiques à la trithérapie d’éradication améliore le taux de succès et réduit les effets indésirables.
Santé mentale et gestion du stress Nouveauté
Les études de 2023-2025 confirment qu’une supplémentation en psychobiotiques (L. helveticus R0052 + B. longum R0175) peut réduire significativement les marqueurs biologiques et subjectifs du stress et de l’anxiété légère après 4 semaines. Une méta-analyse (Zhang et al., BMC Psychiatry, 2023) sur probiotiques, prébiotiques et symbiotiques a démontré des effets positifs mesurables sur les scores de dépression. Ces approches sont complémentaires, non substitutives, aux traitements conventionnels.
Infections respiratoires
Par leur effet immunostimulant, les probiotiques réduisent modérément l’incidence et la durée des infections respiratoires hivernales.
Équilibre intime et prévention des cystites
Les souches L. crispatus, L. gasseri, L. rhamnosus GR-1® et L. reuteri RC-14® restaurent la flore vaginale (bacilles de Döderlein) et préviennent les récidives d’infections génitales. Pour les cystites récidivantes, L. helveticus montre une forte capacité d’inhibition de l’adhésion des uropathogènes.
Prévention oncologique
Les Lactobacillus détruisent des substances précancérigènes (nitrosamines) et inhibent les bactéries productrices d’enzymes activatrices de carcinogènes (β-glucuronidase, azoréductase). La présence en quantité élevée de Fusobacterium nucleatum dans le microbiote est associée au développement du cancer colorectal (Translational Oncology, 2019). Les émulsifiants alimentaires peuvent modifier le microbiote et favoriser une inflammation chronique pro-cancérigène.
Allergie et dermatite atopique
En restaurant la perméabilité intestinale, les probiotiques limitent le passage de protéines imparfaitement digérées, réduisant les phénomènes d’allergie et d’intolérance alimentaire. Des études in vitro montrent une stimulation des cytokines anti-inflammatoires et une diminution des IgE.
Ralentissement du vieillissement
Des études sur des centenaires sardes montrent un microbiote intestinal plus diversifié que la moyenne. La diversité microbienne à l’âge adulte est aujourd’hui identifiée comme un prédicteur de la résilience émotionnelle et cognitive. Une revue de 2025 (15 études, 4 275 participants) confirme un impact des interventions sur microbiote sur la préservation des fonctions cognitives après 45 ans.
Conseils pratiques
Comment prendre les probiotiques ?
• Préférer une prise 15 minutes avant le repas pour limiter l’exposition à l’acidité gastrique
• Ne pas diluer dans des boissons trop chaudes (>40°C) ni glacées : cela détruit les bactéries
• Respecter la chaîne du froid pour les produits réfrigérés
• Ne pas ouvrir les gélules gastrorésistantes
• Un effet bénéfique durable nécessite une cure d’au moins 3 à 4 semaines
Durée de cure recommandée selon l’indication
| 5 à 10 jours Diarrhée aiguë, diarrhée post-antibiotique |
4 à 8 semaines SII, ballonnements, immunité, stress |
3 mois renouvelables Prévention récidives, équilibre intime |
Contre-indications et précautions
|
Immunodépression (cancer, SIDA, corticothérapie prolongée, greffe) : risque rare mais documenté de bactériémie à Lactobacillus ou de fongémie à Saccharomyces boulardii
Allergie aux protéines de lait (allergie vraie, non intolérance) : éviter les probiotiques à base de Bifidus cultivés sur milieu lacté |
Pancréatite aiguë sévère : une étude publiée dans The Lancet a montré une augmentation significative de la mortalité lors de l’utilisation de probiotiques dans ce contexte
Cathéter central / cancers digestifs : contre-indication liée au risque de translocation digestive |
Voies de recherche 2024–2025 Nouveauté
Approche de précision et biomarqueurs fécaux
Les dernières découvertes identifient des biomarqueurs fécaux permettant de personnaliser les interventions probiotiques selon le profil individuel du microbiote. Cette approche de « micronutrition de précision » pourrait permettre d’adapter les souches administrées aux besoins spécifiques de chaque patient.
Microbiote et prise de décision sociale
L’étude de l’Institut du Cerveau (PNAS Nexus, 2024) ouvre des perspectives inédites sur l’influence du microbiote sur les comportements sociaux et la cognition morale. Ces résultats suggèrent que les interventions sur le microbiote pourraient avoir des effets bien au-delà de la sphère digestive.
MICI et Faecalibacterium prausnitzii
Dans la maladie de Crohn, un déficit marqué en Faecalibacterium prausnitzii (principale bactérie productrice de butyrate) est corrélé à la sévérité de la maladie. Des essais explorent son administration directe comme probiotique de nouvelle génération.
Transplantation de microbiote fécal (TMF)
La TMF est désormais validée dans les infections récidivantes à Clostridium difficile et fait l’objet d’études dans la MICI, la dépression résistante et les maladies neurodégénératives. Elle représente l’intervention la plus radicale sur le microbiote intestinal.
📚 Références scientifiques principales
- Falkenstein M. et al. Impact of the Gut Microbiome Composition on Social Decision-Making. PNAS Nexus, Mai 2024. DOI: 10.1093/pnasnexus/pgae166
- Zhang Q. et al. Effect of prebiotics, probiotics, synbiotics on depression. BMC Psychiatry, 2023. DOI: 10.1186/s12888-023-04963-x
- Balasubramanian R. et al. Fermented foods: modulate the microbiota-gut-brain axis for mental health. Neurosci Biobehav Rev, 2024.
- Jiménez-Pareyón G.R. et al. Psychobiotics at the Frontiers of Neurodegenerative Research. Microorganisms, 2025. DOI: 10.3390/microorganisms13122718
- Xiang S. et al. Efficacy of Probiotics for Alzheimer’s, MCI, and Parkinson’s Disease. Front Aging Neurosci, 2022. DOI: 10.3389/fnagi.2022.730036
- Viennois E. et al. Dietary Emulsifiers Directly Impact E. coli Gene Expression. Cell Reports, 2020.
- Wu J., Li Q., Fu X. Fusobacterium nucleatum and Colorectal Cancer. Translational Oncology, June 2019.
- FMC-HGE. Probiotiques dans le SII. POSTU 2024. fmcgastro.org
- Les psychobiotiques, une révolution thérapeutique en devenir. Actualités Pharmaceutiques, Volume 64, 2025.
Anne-Sophie DELEPOULLE (Dr en Pharmacie) — Dernière mise à jour : Avril 2025