Bilan biologique nutritionnel

📋 Sommaire
- Pourquoi réaliser un bilan biologique nutritionnel ?
- Les principales analyses biologiques en micronutrition
- Prescription ciblée selon les grands terrains micronutritionnels
- 3.1. Fatigue / Burn-out / Stress chronique
- 3.2. Inflammation / Stress oxydatif
- 3.3. Digestif / Dysbiose / Hyperperméabilité
- 3.4. Métabolique / Insulinorésistance / Surpoids
- 3.5. Hormonal / Thyroïdien
- 3.6. Sportif / Performance / Récupération
- 3.7. Neuro-cognitif / Humeur / Sommeil
- 3.8. Femme enceinte / Péri-ménopause
- Aspects pratiques et pièges à éviter
- Conclusion
1. Pourquoi réaliser un bilan biologique nutritionnel ?
La micronutrition repose sur le principe que de nombreux troubles fonctionnels chroniques — fatigue persistante, troubles de l’humeur, douleurs diffuses, troubles digestifs, infertilité, troubles cognitifs — trouvent leur origine dans des déséquilibres micronutritionnels infracliniques. Or, ces déséquilibres échappent largement au bilan biologique standard prescrit en médecine générale.
1.1. Objectiver l’invisible
L’interrogatoire alimentaire et clinique, aussi rigoureux soit-il, reste limité par plusieurs biais : déclaration imprécise du patient, variabilité de la biodisponibilité des nutriments, perturbations de l’absorption (dysbiose, hyperperméabilité, achlorhydrie), ou encore augmentation des besoins individuels (grossesse, sport intensif, stress, polymorphismes génétiques). Le bilan biologique permet de passer du subjectif à l’objectif.
Un apport alimentaire théoriquement suffisant ne garantit pas un statut biologique optimal. Par exemple, 20 à 30 % des patients supplémentés en vitamine D à dose « standard » restent en insuffisance biologique, révélant des besoins individuels majorés ou un défaut d’absorption.
1.2. Personnaliser la prise en charge
Le bilan biologique permet d’éviter deux écueils majeurs de la micronutrition :
- La supplémentation « à l’aveugle », souvent inefficace voire contre-productive (risque d’excès en fer, iode, sélénium, cuivre…) ;
- La prise en charge protocolaire standardisée, qui ignore la singularité métabolique de chaque patient.
1.3. Suivre et ajuster
Un bilan de contrôle à 3 à 6 mois permet d’évaluer la réponse à la supplémentation, d’ajuster les posologies, et de détecter d’éventuels effets indésirables (hypervitaminose, surcharge martiale, déséquilibre du ratio zinc/cuivre). C’est également un puissant outil de motivation thérapeutique pour le patient, qui visualise concrètement les progrès réalisés.

1.4. Prévenir les pathologies chroniques
De nombreux déséquilibres micronutritionnels sont désormais identifiés comme facteurs de risque de pathologies chroniques : l’insuffisance en vitamine D et le risque cardiovasculaire, le statut en oméga-3 et les pathologies neurodégénératives, l’insulinorésistance précoce et le syndrome métabolique, le stress oxydatif et le vieillissement accéléré. Le bilan biologique nutritionnel s’inscrit ainsi pleinement dans une démarche de médecine préventive et fonctionnelle.
2. Les principales analyses biologiques en micronutrition
Nous présentons ici les analyses biologiques les plus pertinentes en pratique micronutritionnelle, organisées par grandes familles. Les valeurs de référence indiquées sont les valeurs optimales micronutritionnelles, souvent plus strictes que les seuils de carence « médicale » classiques.
2.1. Bilan martial (statut du fer)
Le fer est un cofacteur enzymatique majeur (synthèse des neurotransmetteurs, respiration mitochondriale, immunité). Son évaluation nécessite plusieurs marqueurs complémentaires, la ferritine seule étant trompeuse.
| Marqueur | Valeur optimale | Interprétation |
|---|---|---|
| Ferritine | Femme : 50–150 µg/L Homme : 80–200 µg/L |
Reflet des réserves. Faussement élevée en cas d’inflammation, syndrome métabolique, alcoolisme. |
| CST (Coefficient de Saturation de la Transferrine) | 25–40 % | Reflet du fer circulant disponible. Abaissé en carence vraie, élevé en surcharge ou hémochromatose. |
| Transferrine | 2,0–3,2 g/L | Augmentée en carence martiale, diminuée en inflammation et dénutrition. |
| Fer sérique | 10–30 µmol/L | Très variable (prélèvement matinal à jeun). Peu fiable isolé. |
| CRP us | < 1 mg/L | Indispensable en parallèle pour interpréter la ferritine. |
Une ferritine à 80 µg/L chez une femme fatiguée avec une CRP à 8 mg/L peut masquer une carence vraie. Toujours interpréter la ferritine à la lumière de la CRP. En cas d’inflammation, se fier davantage au CST.
2.2. Bilan vitaminique
Vitamine D (25-OH-D)
Marqueur central, impliqué dans l’immunomodulation, la santé osseuse, musculaire, cardiovasculaire, et même l’humeur.
- Carence : < 20 ng/mL (50 nmol/L)
- Insuffisance : 20–30 ng/mL
- Optimum micronutritionnel : 40–60 ng/mL (100–150 nmol/L)
- Toxicité : > 100 ng/mL
Vitamine B9 (folates) et B12
Cofacteurs du cycle de la méthylation, impliqués dans la synthèse des neurotransmetteurs, de l’ADN et dans le métabolisme de l’homocystéine.
| Marqueur | Valeur optimale | Commentaire |
|---|---|---|
| Folates sériques | > 10 ng/mL | Reflète apport récent. Folates érythrocytaires plus fiables pour les réserves. |
| Vitamine B12 | > 400 pg/mL | Sous 300 pg/mL : zone grise. Holotranscobalamine et acide méthylmalonique plus spécifiques. |
| Homocystéine | < 10 µmol/L | Marqueur fonctionnel du cycle B9/B12/B6. Élevée : déficit en cofacteurs ou polymorphisme MTHFR. |
L’holotranscobalamine (holoTC) représente la fraction biologiquement active de la B12 (environ 10–30 %). Elle est plus sensible et précoce que la B12 totale pour détecter une carence fonctionnelle. Couplée à l’acide méthylmalonique urinaire et à l’homocystéine, elle constitue le trépied diagnostique de référence du statut en B12.
Autres vitamines
- Vitamine B1 (thiamine) : dosage érythrocytaire, utile chez l’alcoolique chronique, le diabétique, après chirurgie bariatrique.
- Vitamine B6 : pyridoxal-5-phosphate plasmatique (optimal : 30–110 nmol/L). Impliquée dans la synthèse des neurotransmetteurs.
- Vitamines A et E : à rapporter au bilan lipidique pour une interprétation correcte (ratios vit E/cholestérol total).
- Vitamine K : rarement dosée en première intention, sauf contexte particulier (ostéoporose, anticoagulants).
2.3. Bilan en oligoéléments et minéraux
| Élément | Dosage recommandé | Valeur optimale | Intérêt principal |
|---|---|---|---|
| Zinc | Plasmatique + érythrocytaire | Plasma : 12–18 µmol/L | Immunité, peau, fertilité, antioxydant |
| Cuivre | Plasmatique | 12–20 µmol/L | À interpréter avec le zinc (ratio Zn/Cu) |
| Sélénium | Plasmatique ou érythrocytaire | Plasma : 90–130 µg/L | Antioxydant, thyroïde, immunité |
| Magnésium | Érythrocytaire (plus fiable) | 2,0–2,5 mmol/L | Stress, sommeil, crampes, cœur |
| Iode urinaire | Iodurie des 24h ou ratio iode/créatinine | 100–200 µg/L | Thyroïde, grossesse |
| Chrome, manganèse | Plasmatique (cheveux pour Mn) | Spécialisé | Métabolisme glucidique, antioxydant |
Le magnésium sérique ne représente qu’environ 1 % du magnésium corporel total et reste stable même en cas de déficit intracellulaire important. Le dosage érythrocytaire est nettement plus fiable pour évaluer le statut fonctionnel. De même, le zinc et le sélénium peuvent être dosés en érythrocytaire pour une vision plus stable que les seuls taux plasmatiques.
Le ratio zinc/cuivre
Ce ratio est un marqueur fin de l’équilibre oxydatif et inflammatoire :
- Optimal : 1,0 – 1,4
- < 0,8 : profil pro-inflammatoire, déficit relatif en zinc
- > 1,5 : souvent iatrogène (supplémentation excessive en zinc)
2.4. Statut en acides gras (profil des oméga-3 et oméga-6)
L’évaluation du statut en acides gras se fait par chromatographie des acides gras érythrocytaires (membranes plasmiques des globules rouges), reflet fiable de l’intégration membranaire sur 3 à 4 mois.
| Marqueur | Valeur optimale | Signification |
|---|---|---|
| Index oméga-3 (EPA + DHA) | > 8 % | Protection cardiovasculaire, cognitive. < 4 % = risque élevé. |
| Ratio oméga-6 / oméga-3 | < 5 | Régime occidental : souvent 15–20. Objectif : rééquilibrage. |
| Ratio AA / EPA | < 10 | Reflet du potentiel pro-inflammatoire membranaire. |
| Acide α-linolénique (ALA) | > 0,2 % | Apport végétal, conversion limitée en EPA/DHA. |
2.5. Marqueurs du stress oxydatif
Ces marqueurs évaluent l’équilibre entre agressions oxydatives et défenses antioxydantes, enjeu majeur du vieillissement cellulaire et des maladies chroniques.
- Peroxydes lipidiques (MDA, 8-isoprostanes) : marqueurs de peroxydation lipidique.
- 8-OHdG urinaire : reflet de l’oxydation de l’ADN.
- Glutathion (GSH/GSSG) : antioxydant majeur, ratio fonctionnel.
- SOD, GPx érythrocytaires : activité enzymatique antioxydante (sélénium-dépendante pour la GPx).
- Coenzyme Q10 plasmatique : optimal > 0,7 µg/mL. Effondré sous statines.
- Capacité antioxydante totale (CAT, PAO) : vision globale.
2.6. Marqueurs inflammatoires
| Marqueur | Valeur optimale | Intérêt |
|---|---|---|
| CRP ultrasensible (CRP us) | < 1 mg/L | Inflammation de bas grade, risque cardiovasculaire. |
| Fibrinogène | 2–4 g/L | Inflammation chronique. |
| Ferritine (avec CRP) | cf. bilan martial | Protéine de phase aiguë si CRP ↑. |
| Homocystéine | < 10 µmol/L | Inflammation endothéliale, méthylation. |
| Interleukines (IL-6, TNF-α) | Spécialisé | Inflammation de bas grade (laboratoires spécialisés). |
2.7. Marqueurs métaboliques et glucidiques
- Glycémie à jeun : optimal < 0,95 g/L (5,3 mmol/L).
- Insulinémie à jeun : optimal < 7 mUI/L. Permet le calcul du HOMA-IR.
- HOMA-IR = (glycémie × insulinémie) / 22,5 — optimal < 2, insulinorésistance > 2,5.
- HbA1c : optimal < 5,4 %.
- Bilan lipidique complet avec ratios (CT/HDL, TG/HDL) : TG/HDL < 2 est un bon indicateur de sensibilité à l’insuline.
- ApoB et Lp(a) : marqueurs de risque cardiovasculaire plus fins que le LDL isolé.
2.8. Bilan de la méthylation
Le cycle de la méthylation est central en micronutrition (synthèse des neurotransmetteurs, détoxification, régulation épigénétique). Son évaluation repose sur :
- Homocystéine (marqueur fonctionnel principal) ;
- Folates érythrocytaires et B12 active (holoTC) ;
- Génotypage MTHFR (C677T, A1298C) dans certains cas (homocystéine élevée, fausses couches à répétition, troubles de l’humeur résistants).
2.9. Exploration digestive fonctionnelle
Le tube digestif est au cœur de la santé micronutritionnelle (absorption, microbiote, immunité, barrière). Plusieurs analyses sont disponibles, pour la plupart en laboratoires spécialisés :
| Analyse | Ce qu’elle évalue | Indication |
|---|---|---|
| Zonuline sérique ou fécale | Hyperperméabilité intestinale | SII, maladies auto-immunes, troubles cutanés |
| Calprotectine fécale | Inflammation intestinale | Diagnostic différentiel SII vs MICI |
| Élastase pancréatique fécale | Insuffisance pancréatique exocrine | Maldigestion, stéatorrhée |
| Analyse du microbiote intestinal | Dysbiose, diversité, ratios | Troubles digestifs chroniques, terrain inflammatoire |
| sIgA fécales | Immunité muqueuse | Infections récurrentes, dysbiose |
| IgG anti-aliments | Sensibilités alimentaires | Controversé — à utiliser avec recul |
Les tests IgG anti-aliments font l’objet de débats scientifiques. Les sociétés savantes d’allergologie (EAACI) ne recommandent pas leur utilisation en routine diagnostique. Ils peuvent toutefois offrir une piste exploratoire dans certains contextes de sensibilités alimentaires, à condition d’une interprétation prudente et contextualisée.
3. Prescription ciblée selon les grands terrains micronutritionnels
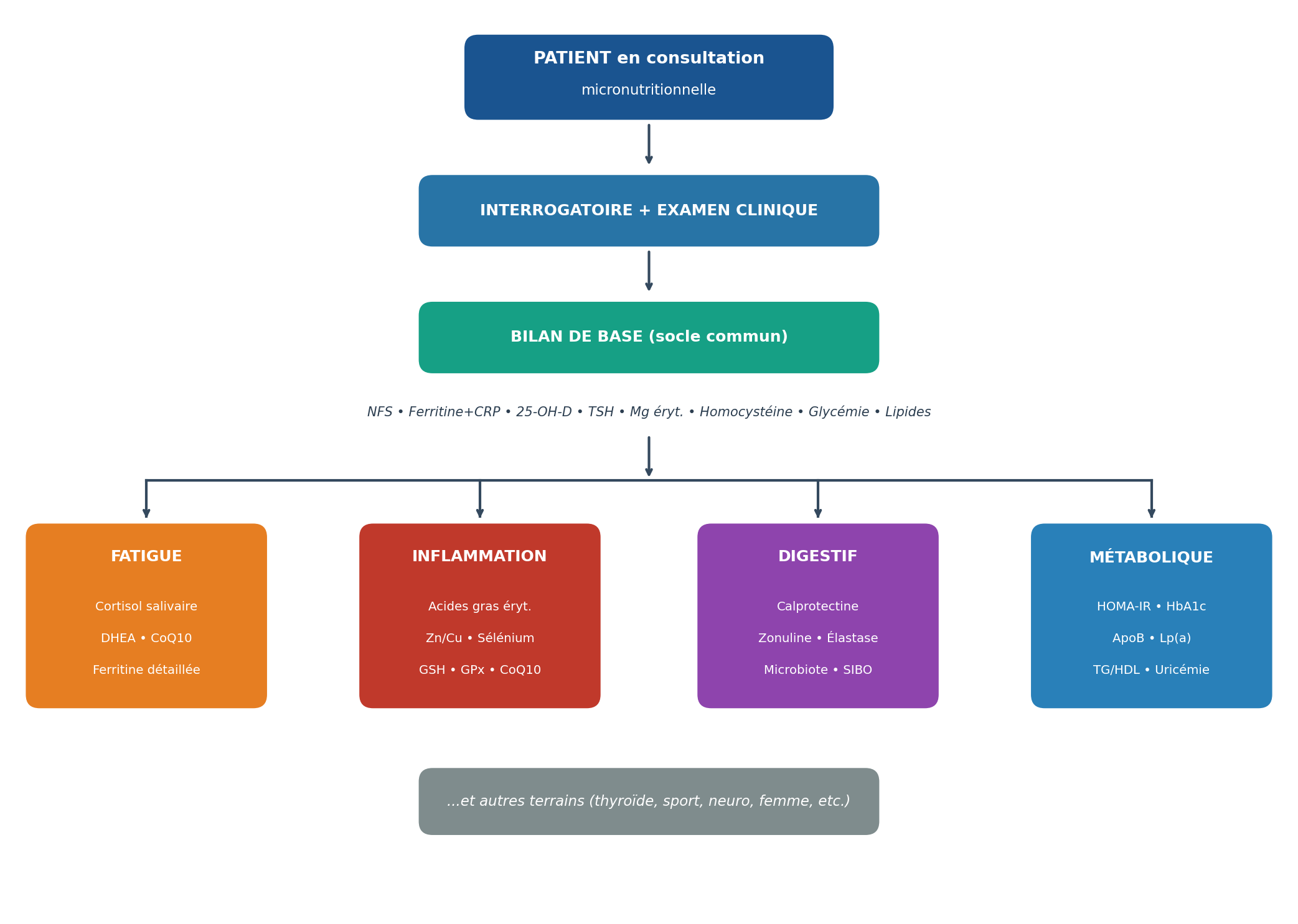
En pratique, la prescription doit être hiérarchisée et proportionnée : un bilan de « débrouillage » de première intention, puis un bilan orienté de seconde intention selon le terrain identifié. Nous proposons ici une approche structurée par grand terrain micronutritionnel.
Bilan de base commun à tous les terrains : NFS, ferritine + CRP us, CST, glycémie à jeun, 25-OH-vitamine D, TSH, magnésium érythrocytaire, homocystéine, bilan lipidique. Ce socle permet déjà de détecter 80 % des déséquilibres majeurs. Le bilan orienté se superpose en fonction du terrain clinique.
3.1. Terrain Fatigue / Burn-out / Stress chronique
Contexte clinique : asthénie persistante, troubles du sommeil, baisse de résistance au stress, troubles de concentration, irritabilité, frilosité, tendance infectieuse.
Bilan recommandé
- 1re intention Bilan martial complet (ferritine, CST, transferrine, CRP us)
- 1re intention 25-OH-vitamine D, magnésium érythrocytaire
- 1re intention TSH, T3 libre, T4 libre
- 1re intention Vitamine B12 (+ holoTC si douteux), folates, homocystéine
- 2e intention Cortisol salivaire (4 points : 8h, 12h, 16h, 22h) — évalue le rythme circadien
- 2e intention DHEA sulfate (ratio cortisol/DHEA)
- 2e intention Coenzyme Q10 plasmatique, carnitine
- 3e intention Neurotransmetteurs urinaires (sérotonine, dopamine) — intérêt discuté
Dans un burn-out installé, on observe souvent un profil de cortisol aplati (pic matinal effondré, cortisol du soir augmenté), une DHEA abaissée, et fréquemment une carence martiale infraclinique masquée (ferritine apparemment « normale » mais inadaptée au contexte inflammatoire). La correction simultanée du terrain martial, magnésien et des rythmes circadiens est souvent déterminante.
3.2. Terrain Inflammatoire / Stress oxydatif
Contexte clinique : douleurs articulaires ou musculaires chroniques, pathologies auto-immunes, maladies cardiovasculaires, vieillissement accéléré, exposition toxique (tabac, pollution, médicaments).
Bilan recommandé
- 1re intention CRP us, fibrinogène, homocystéine
- 1re intention Profil des acides gras érythrocytaires (index oméga-3, ratio O6/O3, AA/EPA)
- 1re intention 25-OH-vitamine D, magnésium érythrocytaire
- 1re intention Zinc, cuivre plasmatiques + ratio Zn/Cu, sélénium
- 2e intention Vitamine E (rapportée au cholestérol), bêta-carotène
- 2e intention Coenzyme Q10, glutathion (GSH/GSSG)
- 2e intention SOD, GPx érythrocytaires
- 3e intention 8-OHdG urinaire, MDA (stress oxydatif avancé)
3.3. Terrain Digestif / Dysbiose / Hyperperméabilité
Contexte clinique : syndrome de l’intestin irritable, ballonnements chroniques, troubles du transit, allergies et intolérances multiples, pathologies auto-immunes, troubles cutanés (eczéma, acné rosacée).
Bilan recommandé
- 1re intention Calprotectine fécale (éliminer une MICI)
- 1re intention Zonuline (sérique ou fécale)
- 1re intention Élastase pancréatique fécale
- 1re intention Vitamine D, B12, folates, fer (statut d’absorption)
- 1re intention Sérologie cœliaque (IgA anti-transglutaminase + IgA totales)
- 2e intention Analyse du microbiote intestinal (séquençage 16S)
- 2e intention sIgA fécales, LPS plasmatiques
- 2e intention Test respiratoire au glucose/lactulose (SIBO)
Un profil fréquent de SII-D (diarrhée prédominante) associe : calprotectine normale, zonuline élevée, ferritine basse, vitamine D insuffisante, B12 limite, dysbiose de fermentation. La prise en charge repose alors sur la réparation de la muqueuse (glutamine, zinc, vitamine A, curcuma), le rééquilibrage du microbiote et l’identification des aliments déclencheurs.
3.4. Terrain Métabolique / Insulinorésistance / Surpoids
Contexte clinique : surpoids abdominal, antécédents familiaux de diabète, syndrome des ovaires polykystiques, fringales sucrées, somnolence postprandiale, hypertension.
Bilan recommandé
- 1re intention Glycémie à jeun, insulinémie à jeun, HOMA-IR
- 1re intention HbA1c
- 1re intention Bilan lipidique complet + ratio TG/HDL
- 1re intention ASAT, ALAT, GGT (stéatose hépatique)
- 1re intention 25-OH-vitamine D, magnésium érythrocytaire
- 1re intention Uricémie, CRP us
- 2e intention ApoB, Lp(a), LDL oxydés
- 2e intention Chrome, zinc, index oméga-3
- 2e intention Score FIB-4 (stéatose hépatique non alcoolique)
3.5. Terrain Hormonal / Thyroïdien
Contexte clinique : troubles du cycle, infertilité, syndrome prémenstruel, hypothyroïdie fruste, goître, thyroïdite auto-immune suspectée.
Bilan thyroïdien complet
- 1re intention TSH, T3 libre, T4 libre
- 1re intention Anticorps anti-TPO et anti-thyroglobuline
- 1re intention Iode urinaire, sélénium plasmatique, zinc
- 1re intention Ferritine + CRP (la carence martiale altère la conversion T4→T3)
- 2e intention T3 reverse (rT3) — si conversion suspectée défaillante
- 2e intention Vitamine D (immunomodulation si Hashimoto)
Bilan hormonal féminin (si indication)
- Œstradiol, progestérone (J21 du cycle)
- FSH, LH, prolactine
- Testostérone totale et libre, SHBG, DHEA-S, Δ4-androstènedione (suspicion SOPK)
- AMH (réserve ovarienne)
Trois micronutriments sont incontournables pour une fonction thyroïdienne optimale : iode (substrat), sélénium (cofacteur des désiodases et de la GPx thyroïdienne), zinc (cofacteur de la conversion T4→T3). Le fer est un quatrième pilier souvent oublié : une ferritine < 50 µg/L suffit à altérer la conversion T4→T3, expliquant certaines « hypothyroïdies fonctionnelles » à TSH normale.
3.6. Terrain Sportif / Performance / Récupération
Contexte clinique : sport d’endurance ou de force, baisse de performance, récupération difficile, blessures à répétition, surentraînement, préparation de compétition.
Bilan recommandé
- 1re intention NFS, bilan martial complet (ferritine souvent basse chez le sportif d’endurance)
- 1re intention Magnésium érythrocytaire, zinc, sélénium
- 1re intention 25-OH-vitamine D, B12, folates
- 1re intention CPK, LDH (adaptation musculaire, surentraînement)
- 1re intention Urée, créatinine, ionogramme
- 2e intention Profil des acides gras érythrocytaires
- 2e intention Testostérone totale et libre, cortisol matinal (ratio T/C)
- 2e intention Bilan du stress oxydatif (CoQ10, GPx, SOD)
- 3e intention Acides aminés plasmatiques (détection de catabolisme, déficit en BCAA)
Le sportif d’endurance présente souvent une pseudo-anémie de dilution (hématocrite abaissé par expansion volémique) et/ou une vraie carence martiale (hémolyse mécanique au niveau plantaire, pertes digestives microscopiques, inflammation). Un CST < 20 % et une ferritine < 30 µg/L chez le sportif doivent alerter même en l’absence d’anémie.
3.7. Terrain Neuro-cognitif / Humeur / Sommeil
Contexte clinique : dépression, anxiété, troubles du sommeil, troubles attentionnels, déclin cognitif, migraines, fibromyalgie.
Bilan recommandé
- 1re intention Vitamine D, B12 + holoTC, folates, homocystéine, B6
- 1re intention Ferritine + CRP, TSH complète
- 1re intention Magnésium érythrocytaire, zinc
- 1re intention Profil des acides gras érythrocytaires (DHA particulièrement)
- 2e intention Cortisol salivaire (rythme), mélatonine salivaire nocturne
- 2e intention Génotypage MTHFR si homocystéine élevée ou dépression résistante
- 3e intention Neurotransmetteurs urinaires (controversé)
- 3e intention Métabolites du tryptophane, kynurénine (inflammation neurologique)
La synthèse de la sérotonine, dopamine et noradrénaline dépend d’un cycle de méthylation fonctionnel. Un déficit en B9, B12, B6 ou un polymorphisme MTHFR peut se traduire par une dépression, une anxiété ou des troubles du sommeil résistants aux traitements classiques. Le dosage de l’homocystéine est un excellent marqueur intégratif de ce cycle.
3.8. Femme enceinte / Péri-ménopause
Grossesse et désir de grossesse
- 1re intention Bilan martial complet (ferritine ≥ 70 µg/L idéalement en préconceptionnel)
- 1re intention Folates érythrocytaires, B12, homocystéine
- 1re intention 25-OH-vitamine D, iode urinaire
- 1re intention TSH, T4 libre, anti-TPO
- 1re intention Glycémie à jeun, HbA1c (dépistage diabète préexistant)
- 2e intention Profil des acides gras (DHA maternel et développement fœtal)
- 2e intention Zinc, sélénium, magnésium érythrocytaire
Péri-ménopause et ménopause
- 1re intention FSH, LH, œstradiol (peu utile en pratique, clinique suffit le plus souvent)
- 1re intention 25-OH-vitamine D, calcium, phosphore, PTH
- 1re intention Marqueurs du remodelage osseux (CTX sérique, ostéocalcine)
- 1re intention Bilan lipidique (profil s’altère à la ménopause), glycémie, HOMA-IR
- 1re intention TSH complète
- 2e intention Homocystéine, CRP us (risque cardiovasculaire)
- 2e intention Magnésium érythrocytaire, vitamines B, index oméga-3
La péri-ménopause constitue une fenêtre d’opportunité majeure en prévention : le profil cardiovasculaire, osseux, glycémique et cognitif se dégrade rapidement avec la chute œstrogénique. Un bilan micronutritionnel complet à ce moment-là, couplé à une prise en charge adaptée (hygiène de vie, supplémentation ciblée, ± THM), peut infléchir durablement la trajectoire de santé.
4. Aspects pratiques et pièges à éviter
4.1. Conditions préanalytiques
- À jeun strict de 12h : glycémie, insulinémie, bilan lipidique, fer sérique, homocystéine.
- Le matin entre 7h et 9h : cortisol sérique, fer, testostérone.
- J21 du cycle : progestérone (si cycle de 28 jours).
- Éviter les 72h post-effort intense pour CPK, ferritine, marqueurs inflammatoires.
- Supplémentation en biotine (vitamine B8) : interfère avec de nombreux dosages immunologiques (TSH, T4L, troponines, 25-OH-D). Arrêter 48h à 72h avant le prélèvement.
4.2. Pièges d’interprétation fréquents
| Piège | Conséquence | Solution |
|---|---|---|
| Ferritine isolée sans CRP | Carence martiale masquée en cas d’inflammation | Toujours coupler à CRP us + interpréter avec CST |
| Magnésium sérique | Faux négatifs fréquents | Privilégier le Mg érythrocytaire |
| B12 « normale » en zone grise | Carence fonctionnelle non détectée | holoTC + acide méthylmalonique + homocystéine |
| TSH seule « normale » | Hypothyroïdie fonctionnelle manquée | Ajouter T3L, T4L, anti-TPO, ferritine |
| Vitamine D au seuil « non carencé » (> 20 ng/mL) | Insuffisance fonctionnelle | Cible micronutritionnelle : 40–60 ng/mL |
| Supplémentation en biotine non arrêtée | Faux résultats TSH, T4L, vitamine D | Arrêt 48–72h avant prélèvement |
| Interprétation hors contexte clinique | Sur- ou sous-diagnostic | Toujours confronter biologie et clinique |
4.3. Coût, remboursement et hiérarchisation
Tous les examens micronutritionnels ne sont pas remboursés par l’Assurance Maladie. Il convient d’informer le patient et de hiérarchiser les prescriptions :
- Largement remboursés : NFS, ferritine, CRP, TSH, bilan lipidique, glycémie, 25-OH-D (sur indication médicale), B12, folates sériques, fer sérique, CST, magnésium.
- Parfois remboursés (selon indication) : homocystéine, HbA1c, anti-TPO, T3L, T4L.
- Non remboursés : magnésium érythrocytaire, holoTC, acides gras érythrocytaires, zonuline, calprotectine (sauf contexte MICI), microbiote, cortisol salivaire, oligoéléments spécialisés, marqueurs du stress oxydatif.
Proposer un bilan « essentiel remboursé » en première intention, puis discuter avec le patient l’intérêt de compléter par quelques analyses spécialisées ciblées (ex. : profil des acides gras érythrocytaires + magnésium érythrocytaire + holoTC, pour environ 150–200 €). Cette approche graduée optimise le rapport information/coût.
4.4. Quels laboratoires ?
Les analyses standards sont réalisables dans tout laboratoire de biologie médicale de ville. Les analyses spécialisées (acides gras érythrocytaires, microbiote, stress oxydatif, neurotransmetteurs, cortisol salivaire) nécessitent le recours à des laboratoires spécialisés en biologie nutritionnelle et fonctionnelle : Barbier, Zamaria, Lims, IMUPRO, Biomnis, Cerballiance Lyon-Nord, certains CHU. Plusieurs de ces laboratoires proposent également un accompagnement à l’interprétation pour les professionnels de santé.
5. Conclusion
Le bilan biologique nutritionnel est aujourd’hui un outil incontournable d’une pratique micronutritionnelle rigoureuse, éthique et efficace. Il permet de quitter l’empirisme, de personnaliser finement la prise en charge, de sécuriser les supplémentations et de suivre objectivement les progrès du patient.
Trois principes guident sa prescription :
- Hiérarchisation : partir d’un socle commun, puis orienter selon le terrain clinique dominant.
- Intégration : toujours interpréter les résultats dans leur contexte, à la lumière de la clinique et des autres marqueurs (par exemple ferritine + CRP, B12 + homocystéine + holoTC).
- Suivi : prévoir un bilan de contrôle à 3–6 mois pour objectiver la réponse et ajuster.
En combinant écoute clinique, bilan biologique ciblé et prise en charge micronutritionnelle personnalisée, le professionnel de santé dispose d’un levier puissant pour accompagner ses patients vers une santé durablement optimisée.
Cet article est destiné aux professionnels de santé. Les valeurs de référence citées correspondent à des optimums micronutritionnels issus de la littérature scientifique et de l’expérience clinique, qui peuvent différer des seuils officiels de carence médicale. Toute prescription et interprétation doivent être personnalisées au contexte individuel du patient.



